دستورالعمل مدیریت تلفیقی حاصلخیزی خاک و تغذیه برنج ( قسمت پنجم)
۶-۱-۳- سیلیسیم
گیاه برنجی با تولید ۵ تن در هکتار دانه حدود ۴۷۰-۲۳۰ کیلوگرم سیلیسیم عنصری را از یک هکتار زمین برحسب نوع خاک و رقم جذب می نماید. آزمایش خاک و گیاه برای ارزیابی کمبود سیلیسیم می تواند انجام شود. سطح بحرانی سیلیسیم در خاک برای وقوع کمبود، ۴۰ میلی گرم سیلیسیم در کیلوگرم خاک با عصاره گیر استات سدیم یک مولار در pH برابر ۴ می باشد. دلایل عمده کمبود سیلیسیم در خاک شامل قدرت ذخیره سازی سیلیسیم کم خاک ناشی از هوادیدگی شدید و فرسودگی خاک، کمبود سیلیسیم در مواد مادری و تخلیه سیلیسیم از خاک در اثر کشت متراکم و برنگرداندن بقایا به خاک می باشد. مقدار کم سیلیسیم در خاک مشخصه پایین بودن حاصلخیزی خاک اراضی شالیزاری است (سیلیسیم عنصری حساس به آبشویی می باشد). خاکهایی که از لحاظ مقدار سیلیسیم پایین هستند به طور معمول از نظر عناصر غذایی دیگر نیز فقیر می باشند. به جزء خاکهای آتشفشانی که اغلب غنی از سیلیسیم بوده و از نظر فسفر، کلسیم و منیزیم فقیر هستند وضعیت سیلیسیم در گیاه برنج شاخص عمومی وضعیت تغذیه ای محسوب میشود، به دلیل اینکه مصرف سیلیسیم معمول نمی باشد، و در اثر کشت متراکم، مقادیر بالایی از کاه و کلش برداشت میشوند، بالانس سیلیسیم اغلب منفی (۳۵۰-۱۵۰ کیلوگرم سیلیسیم در هكتار) بوده و کمبود سیلیسیم ممکن است در آینده در این سیستمها گسترش یابد. خاکهایی که در معرض کمبود سیلیسیم هستند دارای خصوصیات زیر میباشند:
خاکهای شالیزار قدیمی در مناطق معتدله (مثل ژاپن و کره) یا نیمه حاره (مثل شمال ویتنام)، خاکهای آلی با مقادیر کم سیلیسیم معدنی (مثل پیت در فلوریدا، اندونزی، و ماداگاسکار)، خاکهای به شدت هوا دیده و آبشوئی شده مناطق حاره (مثل شمال شرق تایلند).
اصول مدیریتی:
مقداری از سیلیسیم از طریق آب آبیاری وارد می شود. به ویژه اگر آب زیرزمینی از مناطقی که دارای سنگهای آتشفشانی باشند بگذرد. با فرض غلظت سیلیسیم ۳-۸ میلی گرم سیلیسیم در لیتر و در حدود ۱۰۰۰ میلی متر آب آبیاری، سیلیسیم ورودی از طریق آب آبیاری در حدود ۸-۳۰ کیلوگرم در هکتار می باشد. در طی مدت طولانی، کمبود سیلیسیم با برگرداندن کاه و کلش به مزرعه اتفاق نمی افتد. کاه و کلش برنج ۶-۵ درصد سیلیسیم و پوسته برنج ۱۰ درصد سیلیسیم دارند. در شرایط کمبود سیلیسیم ممانعت از کاربرد مقادیر اضافی از کودهای نیتروژنی که موجب افزایش عملکرد و جذب کل نیتروژن و سیلیسیم شده در نتیجه کاهش غلظت سیلیسیم در کاه و کلش را به دنبال دارد ممانعت گردد. رفع کمبود سیلیسیم با کاربرد سیلیکات کاسیم و اسید سیلیسیک امکان پذیر است.
۷-۱-۳- توصیه کاربرد عناصر کم مصرف
روی
کمبود روی در خاکهای آهکی، سدیمی، خاکهای دارای pH بالا، هیستوسل، خاکهای شنی، لومی شنی، لومی و آلی (نسبت به خاکهای سیلتی یا رسی) و نیز خاکهایی که برای مدت طولانی مرطوب بوده اند شایع تر است. همچنین خاکهای دارای مقدار بالای سیلیسیم محلول در آب و خاکهایی که نسبت منیزیم به کلسیم بیش از یک دارند کمبود روی از خود نشان می دهند. ساده ترین روش برای برطرف کردن کمبود روی زهکشی کردن مزرعه و در نتیجه افزایش حلالیت روی می باشد. اما این روش اغلب به دلیل اثرات مفید غرقاب طولانی مدت برای کشت برنج غیرممکن یا نامطلوب است. کمبود روی را بوسیله غوطه ور کردن نشاهای برنج درسوسپانسیون ۲ درصد اکسید روی در آب می توان برطرف نمود. به علاوه مقدار ۲۵ کیلوگرم در هکتار سولفات روی را می توان با ۵۰ کیلوگرم شن خشک مخلوط کرده و در یک هکتار به کار برد. این مقدار را نیز می توان به نسبت ۱:۱۰ با کود دامی پوسیده مخلوط کرده و با رطوبت مناسب به مدت ۳۰ روز رها نمود. این مخلوط قبل از کشت مصرف می گردد. در صورت کاربرد کود سبز (۶/۵ تن در هکتار) مقدار 12/5 کیلوگرم در هکتار سولفات روی کافی است. در صورت مشاهده علایم کمبود روی، برنج با محلول حاوی ۰/۵ درصد سولفات روی و یک درصد اوره با فاصله ۱۵ روز یک بار تا زمان رفع کمبود محلول پاشی می گردد. محلول پاشی در زمان پنجه زنی تا گلدهی می تواند مؤثر باشد.
آهن
برای تایید کمبود آهن می توان هم خاک و هم گیاه را آزمایش نمود. به منظور بررسی وضعیت تغذیه ای آهن، مقدار آهن فعال برگ از مقدار کل آهن شاخص مناسب تری می باشد. حد بحرانی آهن در ۲۰ روز بعد از کاشت ۲۵ میلی گرم در کیلوگرم در بافت برگ می باشد. حد بحرانی آهن در مناطق مریستمی دارای رشد سریع، بسیار بالاتر است. در بافتهای رویشی مثل ساقه ها، حد بحرانی آهن در حدود ۲۰۰ میلی گرم در کیلوگرم برای آهن کل و ۸۰-۶۰ میلیگرم در کیلوگرم برای آهن فعال می باشد. حد بحرانی آهن در خاک ۲ میلی گرم در کیلوگرم با عصاره گیر استات آمونیوم و ۲-۵ میلی گرم در کیلوگرم برای عصاره گیر DTPA تعیین شده است. غلظت کم 2+ Fe در محلول خاک اراضی بالادست، شرایط احیای ناکافی خاک در شرایط غرقابی (به طور مثال خاکهای با ماده آلی کم)، خاکهای با pH بالا یا قلیایی یا خاکهای آهکی (کاهش حلالیت و جذب آهن به دلیل غلظت بالای بی کربنات)، نسبت فسفر به آهن بالا در خاک و ترکیب آهن به صورت فسفاتهای آهن در اثر کاربرد مقادیر بالای فسفر، غلظت بالای منگنز، مس، روی، مولیبدن، نیکل و آلومینیوم در خاک، کشت ارقام با پتانسیل کم برای ترشح اسیدهای آلی که آهن را قابل حل می کنند و افزایش pH ریزوسفر بعد از کاربرد مقادیر بالای کودهای نیتروژنی یا نیتراتی از عوامل مؤثر در کمبود آهن در کشت برنج می باشد. در خاکهای قلیایی، غیر متحرک شدن آهن در ریشه های گیاه به دلیل رسوب آهن اتفاق می افتد. به دلیل اینکه آهن در بافت گیاهی برنج غیرمتحرک است، علایم کمبود آن ابتدا در برگهای جوان اتفاق می افتد.
مدیریت کمبود آهن:
انتخاب و اصلاح ارقام متحمل به کمبود آهن، کاربرد مواد آلی، استفاده از کودهای حاوی آهن . در مقطع فعلی کمبود آهن در مزارع برنج در شمال کشور نه تنها مطرح نمی باشد، بلکه مسمومیت آن تحت شرایطی مساله ساز شده است.
سمیت آهن:
در شرایط غرقابی به دلیل احیای آهن، غلظت بالایی از آهن قابل جذب در محلول خاک تجمع می یابد که ممکن است به سمیت آهن منجر شود. در شرایط سمیت آهن، نقاط قهوه ای باریک روی برگهای قدیمی تشکیل می شود. این نقاط از نوک برگ شروع شده و به طرف انتهای برگ گسترش می یابد. نقاط در بین رگبرگها به هم پیوسته شده و برگها رنگ قهوه ای نارنجی پیدا کرده و در نهایت می میرند. برگها باریک شده اما اغلب سبز باقی می مانند. در بعضی واریته ها نوک برگها به رنگ زرد نارنجی در آمده و خشک می شوند. با پوششی قهوه ای تیره روی سطح ریشه، ریشه ها آسیب دیده و می میرند. برای تشخیص سمیت آهن هم آزمایش خاک و هم گیاه می تواند انجام شود. دامنه مناسب و سطح بحرانی برای وقوع سمیت آهن دریافت گیاهی به شرح (۱۷) می باشد.
به طور معمول مقدار آهن در گیاهان دچار مسمومیت بالا بوده (۲۰۰۰-۳۰۰ میلیگرم در کیلوگرم) اما مقدار بحرانی آن بستگی به سن گیاه و وضعیت تغذیه ای آن دارد. مقدار بحرانی آن در خاکهای فقیر و در شرایطی که بالانس تغذیه ای مناسب نیست، پایین می باشد. در گیاهان دچار مسمومیت آهن مقدار پتاسیم برگ پایین می باشد (کمتر از یک درصد) و نسبت K:Fe کمتر از ۱: ۱۸-۱۷ در اندام هوایی و ۱: 1/5 در ریشه ها می باشد که ممکن است سمیت آهن را مشخص نماید. غلظت بحرانی آهن در محلول خاک برای وقوع سمیت آن دارای دامنه وسیعی است. گزارشها حاکی از دامنه ۱۰۰-۱۰ میلی گرم آهن در لیتر محلول خاک است که مشخص می نماید سمیت آهن تنها به غلظت آن در محلول خاک بستگی ندارد. اختلاف بین غلظت بحرانی آهن در محلول خاک به اختلاف در ریشه های ارقام مختلف برنج برای کاهش اثرات سمیت آهن بستگی دارد. غلظت بالای +Fe2 در محلول خاک به دلیل شرایط احیای شدید در خاک یا در PH پایین، وضعیت ضعیف عناصر غذایی یا عدم بالانس آنها، اکسیداسیون ضعیف ریشه و قدرت ترشح کم 2+Fe به دلیل کمبود پتاسیم، منیزیم، کلسیم و فسفر، کمبود پتاسیم همراه با درصد اشباع بازی کم خاکی و کاربرد فاضلابهای صنعتی یا کشاورزی غنی از آهن از دلایل عمده سمیت آهن محسوب می شود.
– مکانیسم عارضه:
سمیت آهن ابتدا به دلیل اثرات سمی جذب آهن اضافی در اثر غلظت بالای آهن در محلول خاک اتفاق می افتد. آهن اضافی به علت افزایش نفوذپذیری ریشه و افزایش احیای میکروبی آهن در ریزوسفر ریشه گیاهان، جذب میشود. جذب آهن اضافی منجر به افزایش فعالیت پلی فنل اکسیداز شده و برگها برنزه می شوند. مقادیر بالای آهن در گیاه موجب افزایش تشکیل رادیکالهای اکسیژن می گردد. رادیکالهای آزاد اکسیژن به شدت فعال بوده و عامل اصلی برای تجزیه پروتئینها و چربیهای غشاء سلول هستند. واریته های برنج نسبت به سمیت آهن حساسیت متفاوت دارند. مکانیسمهای اصلی تطابق گیاهان برای مقابله با سمیت آهن شامل اکسیداسیون + Fe2 در ریزوسفر ریشه و ممانعت از جذب اضافی 2+Fe و رسوب Fe+3 به وسیله ریشه ها (پوششی قهوه ای قرمز روی ریشه ها) می باشد، در خاکهای به شدت احیا شده که مقادیر بالایی از آهن دارند، ممکن است اکسیژن کافی برای اکسیداسیون 2+Fe در سطح ریشه وجود نداشته باشد. در چنین شرایطی، جذب آهن زیاد شده و سطح ریشه ها به دلیل حضور سولفید آهن سیاه می شود. زمانی که ذخیره عناصر غذایی (Ca، P ،Si ،K و Mg) پایین است و مقادیر بالایی از ترکیبات سمی مثل H2S وجود دارد، قدرت اکسیداسیون ریشه کاهش می یابد. سمیت آهن با چند عامل محدودیت تغذیه ای که منجر به کاهش قدرت اکسیداسیون ریشه می شود ارتباط دارد. ریشه های گیاهان دچار کمبود پتاسیم، فسفر، کلسیم و یا منیزیم، متابولیتهای بیشتری با وزن مولکولی کم (مثل قندهای محلول، آمیدها، اسیدهای آمینه) ترشح می کنند. در دوره شدت فعالیت متابولیکی (بطور مثال جوانه زنی)، ترشح این متابولیتها منجر به افزایش جمعیت ریزجانداران شده که موجب افزایش تقاضا برای قبول کنندهای الکترون می شود. در چنین شرایطی، باکتریهای غیرهوازی اجباری و اختیاری آهن، 3+Fe را به 2+Fe تبدیل می کنند.
مدیریت کاهش سمیت آهن:
کاشت واریته های متحمل به مسمومیت آهن با قدرت اکسیداسیون بالای ریشه و ذخیره کافی عناصر غذایی در گیاه از مهمترین راه های کاهش اثرات سمی غلظتهای بالای آهن می باشد. در آب و هوای معتدل که بذر به طور مستقیم کشت می شود، بذرها با اکسید کننده های شیمیایی مثل کلسیم پراکسیداز به مقدار ۵۰ تا ۱۰۰ درصد وزن بذر برای بهبود جوانه زنی و پایداری نشاء پوشش داده می شود. دیگر راههای کاهش سمیت آهن شامل موارد زیر است:
- تاخیر در کاشت تا زمانی که حداکثر غلظت آهن در محلول خاک گذشته باشد (به طور مثال ۱۰ تا ۲۰ روز بعد از غرقاب).
- آبیاری متناوب و ممانعت از غرقاب دائمی در خاکهای با زهکشی ضعیف که مقادیر بالایی از غلظت آهن و مواد آلی دارند.
- برقراری بالانس عناصر غذایی، مصرف مقادیر مناسبی از کودهای پتاسیم، فسفر و منیزیم.
- انجام شخم خشک بعد از برداشت برنج به منظور افزایش اکسیداسیون در طی دوره شخم. این عمل موجب کاهش غلظت 2+Fe در طی دوره غرقاب بعدی می شود.
- افزایش pH خاکهای اسیدی با آهک دهی.
- مصرف ۲۰۰-۱۰۰ کیلوگرم در هکتار اکسید منگنز (MnO2) در خاک سطحی برای کاهش احیای Fe+3 .
- جلوگیری از مصرف بالای مواد آلی (کود دامی و گیاهی) در خاکهای با مقادیر بالای آهن و زهکشی ضعیف.
- استفاده از اوره به جای سولفات آمونیوم
- انجام زهکشی وسط فصل برای کاهش تجمع Fe+2 . در ۳۰-۲۵ روز بعد از کاشت، زهکشی مزرعه و نگه داشتن آن به صورت مرطوب حدود ۱۰-۷ روز، ذخیره اکسیژن خاک را در مرحله پنجه زنی افزایش می دهد.
منگنز
نسبت Fe:Mn بیش از ۱: 2/5 در اندام هوایی در مراحل اولیه رشد (پنجه زنی) نشانه کمبود منگنز می باشد. مصرف منگنز برای خاکهای با منگنز بیش از ۴۰ میلی گرم در کیلوگرم با عصاره گیر ( HCl ) 0/1 مولار و بیش از ۵ میلی گرم در کیلوگرم با عصاره گیر DTPA توصیه نمی شود. دامنه مناسب غلظت منگنز در محلول خاک ۳۰-۳ میلی گرم در کیلوگرم می باشد. مقدار منگنز قابل استفاده کم در خاک، غلظت بالای آهن در خاک، افزایش غلظت Zn+2 و Mg2+ ، Ca+2 , و 4+NH در محلول خاک و تجمع سولفید هیدروژن از دلایل عمده کمبود منگنز می باشد. کمبود منگنز به طور معمول در اراضی خشکه کاری برنج مشاهده میشود ولی در اراضی پایین دست با غرقاب طولانی به دلیل افزایش حلالیت منگنز در شرایط غرقاب معمول نمی باشد .انواع خاکهایی که در معرض کمبود منگنز هستند شامل :
خاکهای اسیدی خشکه کاری (التی سلها و اکسی سل ها)، خاکهای قلیایی و آهکی با مواد آلی کم و مقدار منگنز قابل استفاده کم، خاکهای غرقابی هوادیده حاوی مقادیر بالای آهن فعال، خاکهای شنی و شسته شده با مقادیر منگنز پایین می باشد. در مقطع فعلی کمبود منگنز در مزارع برنج در شمال کشور نه تنها مطرح نمی باشد، بلكه مسمومیت آن نیز تحت شرایطی مسئله ساز می باشد.
سمیت منگنر:
سمیت منگنز می تواند بوسیله آزمایش خاک و گیاه اثبات شود. سطح بحرانی برای وقوع سمیت منگنز در برگ جوان برنج و یا در ساقه آن در هنگام پنجه زنی بیش از ۸۰۰ -۲۵۰۰ میلی گرم در کیلوگرم می باشد سمیت منگنز به طور معمول با سمیت آلومینیوم همزمان می شود. غلظت بالای منگنز در محلول خاک به دلیل pH پایین خاک (کمتر از ۵/۵)، پتانسیل اکسیداسیون و احیای پایین، وضعیت ضعیف و غیر متعادل عناصر غذایی، افزایش حلالیت Fe+2 به دلـیل کـمـبود Ca, P, K ،Si و یا Mg ، ممانعت از انـجام تعـرق از طـریق تولیـد H2S و FeS و اسیدهای آلی و مصرف پسماندهای صنعتی غنی از منگنز از دلایل بروز علایم سمیت منگنز در برنج می باشد. سمیت منگنز به ندرت در اراضی شالیزاری واقع می شود. برخلاف غلظت بالای منگنز در محلول خاک به دلیل تحمل برنج به غلظت بالای این عنصر سمیت منگنز اهمیت چندانی ندارد. ریشه های برنج قادر به خروج منگنز از سلولهای خود بوده و در این صورت بافتهای گیاهی تحمل بالایی نسبت به غلظت منگنز در محلول خاک دارند. مقدار بالای منگنز در بافت گیاهی موجب تغییر فرآیندهای متابولیسمی (فعالیت آنزیمی و ترکیبات آلی) و ظهور علایم مسمومیت مثل کلروز (اکسیداسیون نوری کلروفیل) یا نکروز (تجمع ترکیبات فنلی اکسید شده مثل آنتوسیانین) می شود. واریته های برنج نسبت به سمیت منگنز حساسیت متفاوت دارند. واریته های مقاوم ، منگنز بیشتری را در ریشه خود نگه می دارد. آزاد کردن اکسیژن از ریشه ها برای اکسیداسیون Mn+2 در ریزوسفر، اختلاف در آناتومی و مورفولوژی ریشه و ذخیره مناسب از عناصر غذایی Ca, P ،Si, K و Mg قدرت اکسیداسیون ریشه را تحت تأثیر قرار می دهد.
مدیریت سمیت منگنز:
پوشش دار کردن بذر با اکسیدانت (مانند کلسیم پراکسیداز) برای بهبود جوانه زنی و استقرار نشاء بوسیله افزایش ذخیره اکسیژن در اطراف ریشه از راههای کاهش سمیت منگنز میباشد. برقراری تعادل تغذیه ای و کاربرد مقادیر کافی کودهای پتاسیمی، استفاده از کودهایی که خاصیت اسیدزایی کمتری دارند (مثل اوره) از دیگر روشهای کاهش اثرات سمی منگنز می باشد. جذب منگنز در حضور یون آمونیم نسبت به نیترات کاهش می یابد. برگردندان بقایا به منظور جایگزینی سیلیسیم و پتاسیم برداشت شده از مزرعه و ذخیره مناسب از سیلیسیم در گیاه به منظور کاهش در جذب منگنز، سمیت آن را کنترل می کند.
مس
سطح بحرانی برای وقوع کمبود مس در خاک با عصاره گیر (HCI ) 0/1 میلی گرم در کیلوگرم و با عصاره گیر DTPA برابر با 0/3-0/2 میلی گرم در کیلوگرم می باشد. مقادیر مس قابل استفاده کم در خاک، جذب قوی مس بوسیله اسیدهای هیومیک و فولویک (خاکهای پیت)، مقادیر کم مس در مواد مادری (خاکهای شنی دارای منشاء کوارتز)، میزان بالای کاربرد کودهای حاوی عناصر پرمصرف و در نتیجه رشد سریع گیاه و کم شدن مس در محلول خاک، آهک دهی بیش از حد خاکهای اسیدی، افزایش مقادیر کمپلکس شده مس بوسیله مواد آلی یا جذب شده و محبوس شده بوسیله اکسیدها و هیدروکسیدها و مقادیر بالای روی در خاک از دلایل عمده کمبود مس به حساب می آید.
کمبود مس در خاکهای زیر به وقوع می پیوندد:
خاکهای با مواد آلی بالا (هیستوسل، خاکهای با خاکسترهای آتشفشانی)، لاتریتها و خاکهای با هوادیدگی بالا (التی سل و اکسی سلها)، خاکهای دارای منشاء رسوبات دریایی (لایم استن ها)، خاکهای با بافت شنی و خاکهای آهکی .
فرو بردن ریشه های نشاء در سوسپانسیون یک درصد سولفات مس به مدت یک ساعت قبل از کاشت، ممانعت از آهک دهی زیاد خاک به منظور کاهش جذب مس ، کاربرد اکسید مس و سولفات مس به میزان ( ۵ تا ۱۰ کیلوگرم در هکتار هر ۵ سال یکبار) برای نگهداری مس قابل استفاده خاک در حد مناسب و به مدت طولانی (به روش پخش سطحی و یا مخلوط با خاک) از روشهای معمول در رفع کمبود مس محسوب می شود. سولفات مس به شدت آب دوست بوده و ممکن است در صورت اختلاط با کودهای پرمصرف مثل فسفر تشکیل ترکیبات نامحلول دهد. کودهای مسی دارای اثرات باقیمانده زیاد هستند. در مقطع فعلی کمبود مس در مزارع برنج در شمال کشور چندان محدود کننده عامل رشد نمی باشد.
بور
کمبود بر صورت خیلی نادر به ویژه در سیستم کشت اراضی آبی برنج اتفاق می افتد. برای برنج این عارضه خیلی نادر بوده ولی در خاکهای به شدت هوا دیده، خاکهای اسیدی قرمز و خاکهای شنی به وقوع می پیوندد. در مقطع فعلی کمبود بور در مزارع برنج در شمال کشور چندان محدود کننده عامل رشد نمی باشد.
مدیریت کمبود بور:
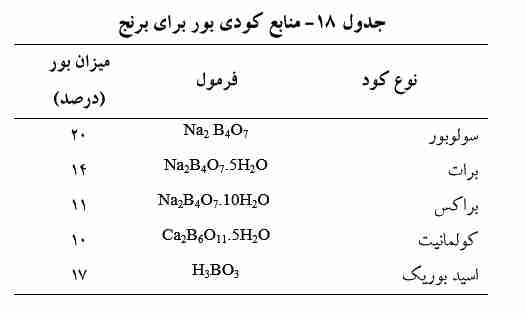
به دلیل تحرک بالای بور در اراضی شالیزاری مدیریت آب و جلوگیری از آبشویی می تواند در عدم بروز کمبود بور مؤثر باشد. سطح بحرانی غلظت بور در خاک به روش آب داع 0/5 میلی گرم در کیلوگرم می باشد. سطح بحرانی آن بسته به عصاره گیرهای مختلف در دامنه 0/7-0/1 میلی گرم در کیلوگرم متغیر است. در خاکهای دچار کمبود بور، از منابع کندرهای بور مثال کولمانیت ( ۲۰ تا ۳۰ کیلوگرم در هكتار در خاکهای سیلتی و رسی و ۲۰ تا ۵۰ کیلوگرم در هکتار در خاکهای شنی) به فاصله ۲ تا ۳ سال یکبار استفاده شود. کودهای حاوی بور در خاکهای سیلتی و رسی دارای اثرات باقیمانده زیادی نسبت به خاکهای شنی می باشد. در سیستم تناوبی برنج – گندم، کاربرد بور در زراعت گندم، مقدار نیاز زراعت برنج را نیز برطرف می نماید. کاربرد فرم های محلول بور مانند اسید بوریک (۳-0/5 کیلوگرم بور در هکتار) و یا براکس برای رفع سریع کمبود بور به صورت پخش سطحی و مخلوط با خاک قبل از کاشت و همچنین مصرف سرک یا محلول پاشی در طی رشد رویشی گیاه برنج توصیه میشود. براکس و دیگر کودهای بور نبایستی با یکدیگر مخلوط شوند. در جدول (18) مشخصات منابع کودى بور نشان داده شده است.
سمیت بور:
غلظت بالای بور در محلول خاک به دلیل استفاده از آب زیرزمینی غنی از بور و با درجه حرارت بالا (به طور مثال در مناطق خشک، بالا آوردن آب از اعماق خیلی زیاد، یا در مناطق با فعالیتهای آتشفشانی) و یا به دلیل وجود مواد مادری غنی از بور در خاک (مقدار بور در بعضی از رسوبات دریایی، سنگهای آذرین درونی و دیگر مواد آتشفشانی بالاست اما مقدار آن در سنگهای آذرین بیرونی پایین است) مشاهده می شود. استفاده زیاد از کود براکس با مواد کمپوستی از جمله دلایل وقوع سمیت بور میباشد . سمیت بور در مناطق خشک و نیمه خشک معمول بوده اما در شالیزارهای دیگر مناطق نیز گزارش شده است. فیزیولوژی تحمل و مسمومیت بور هنوز به خوبی شناخته نشده است. جذب بور توسط گیاه در ارتباط نزدیک با غلظت آن در محلول خاک و میزان تعرق گیاه دارد. وقتی غلظت بور در محلول خاک بالاست در تعرق معمول، بور به مقدار زیاد جذب گیاه شده که موجب تجمع آن در حاشیه و نوک برگها می شود. بور اضافی از تشکیل نشاسته از قندها ممانعت به وجود آورده و موجب تشکیل کمپلکسهای بور- کربوکسیلات و تاخیر در پرشدن دانه می گردد. در این شرایط رشد رویشی گیاه طبیعی است.
اصول مدیریتی برای کاهش اثرات سمیت بور
- کاشت واریته های متحمل به سمیت بور، واریته های متحمل به سمیت بور می توانند عملکردی بیشتر از ۲ تن در هکتار نسبت به واریته های حساس داشته باشند.
- استفاده از آبهای سطحی با غلظت بور کم. اگر از آبهای زیرزمینی استفاده می شود، به طور منظم غلظت بور پایش شود. اگر غلظت بور بیش از حد معمول باشد با آب با غلظت کم بور رقیق شده و سپس مصرف شود.
- زمانی که خاک خشک است به دلیل اینکه بور در خاک سطحی تجمع می یابد، شخم زده شده و با آب با غلظت کم بور آبشویی شود.
۲-۳- کاربرد کودهای زیستی در زراعت برنج
کودهای زیستی به مواد جامد (بیشتر بودری)، مایع و یا در برخی موارد ژله مانند اطلاق می شود که قادرند جمعیت انبوه از یک یا چند نوع ارگانیسم مفید خاکزی و یا فرآورده متابولیک آنها را روی یک ماده نگهدارنده یا حامل از زمان تولید تا زمان مصرف نگهداری نماید. این دسته از کودها به منظور تأمین عناصر غذایی مورد نیاز گیاهان و یا افزایش رشد و عملکرد آنها، استفاده می شوند. انواع متفاوتی از کودهای زیستی امروزه در دنیا معرفی شده است که توسط زارعین برای کشت مورد استفاده قرار می گیرد. کودهای زیستی حاوی باکتریهای محرک رشد گیاه از مهمترین انواع کودهای زیستی قابل استفاده در کشت برنج می باشند. باکتریهایی مانند سودوموناس، باسیلوس، هرباسپیربلوم، از توباکتر و آزوسپیربلوم از انواع شناخته شده باکتریهای محرک رشد گیاه می باشند. باکتریهای محرک رشد گیاه به وسیله مکانیسمهای مختلف، به طور مستقیم و یا غیر مستقیم رشد گیاهان را افزایش می دهند. مکانیسمهای مستقیم شامل تثبیت زیستی نیتروژن، حلالیت فسفاتهای نامحلول، تولید تنظیم کننده های رشد و ویتامینها می باشند که با اثرات مستقیم بر رشد گیاه سبب افزایش عملکرد گیاهان می باشند. از مکانیسمهای غیر مستقیم می توان به خصوصیاتی مانند تولید سیانید، آنتی بیوتیکها و سیدروفورها اشاره کرد. مکانیسمهای غیر مستقیم با تعلیل اثرات منفی تنش های زنده و غیر زنده سبب بهبود رشد گیاهان می شوند.
نحوه مصرف کودهای زیستی محرک رشد گیاه در برنج:
مقدار و نحوه مصرف کودهای زیستی محرک رشد گیاه بستگی زیادی به نوع فرمولاسیون آنها دارد. این کودها بیشتر به شکل مایع و یا پودری تولید می شوند. حسب نوع فرمولاسیون هر کود نحوه مصرف آن به شرح زیر می باشد.
الف کودهای بیولوژیک محرک رشد گیاه با فرمولاسیون مایع
۱- بذر مال:
ابتدا مقدار معینی از بذر داخل ظرف مناسب تمیزی ریخته می شود. سپس متناسب با مقدار بذر مصرفی، کود زیستی مایع به آن اضافه شده و برای چند دقیقه محتویات ظرف به خوبی تکان داده میشود تا از آغشته شدن کلیه بذور به کود زیستی اطمینان حاصل گردد. سپس بذرها برای کاشت آماده هستند. در صورت آماده نبودن شرایط کاشت، بذرها در مکان مناسب تمیزی (دور از نور مسقیم خورشید و هوای سرد و خشک) نگهداری می شوند. نگهداری بذور در این شرایط بیش از ۲۴ ساعت توصیه نمی شود. مقدار کود زیستی مایع مصرفی بستگی به میزان و نوع بذر دارد. در مورد برنج به ازای هر یک کیلوگرم بذر کاربرد ۱۰۰ میلی لیتر از مایه تلقیح مایع توصیه می گردد.
۲ – خزانه ای:
در گیاهان خزانه ای مانند برنج پیشنهاد می شود که قبل از کاشت بذر در خزانه با روش بذرمال تلقيح گردند. سپس در هنگام انتقالات به زمین اصلی نیز تلقیح انجام می شود. در این روش در هنگام انتقال نشا به مزرعه ، مجموعه ای از چندین بوته را از خزانه جدا کرده و ریشه های آنها را به خوبی می شویند تا اثری از ذرات خاک وجود نداشته باشد. سپس ظرف تمیز مناسبی را تهیه کرده و کود زیستی مورد نظر را به داخل آن منتقل می کنند. پس از آن ریشه گیاه به مدت ۲۰ دقیقه داخل محلول کود نگهداری می شود. مقدار کود مصرفی بستگی زیادی به حجم ریشه گیاه مورد نظر دارد. در صورتی که جمعیت میکروارگانیسمهای موجود در کود پایه ای از ده به توان 8 یا ده به توان نه باشد می توان به ترتیب تا ده و صد بار کود را با آب تمیز غیر کلره و ترجیحاً جوشانده شده رقيق نمود. برای نتیجه بهتر توصیه می شود قبل از انتقال گیاه به ظرف حاوی کود، کود مورد نظر را با مقدار معینی از مواد مخلوط ، چسبناک نموده و پس از اطمینان از حل شدن کامل و یکنواخت چسب در آن، گیاه به ظرف مورد نظر منتقل شود. برای رقیق سازی، از کودهای زیستی با جمعیت پایه ۱۰ به توان7 و انواعی که بیش از دو ماه از تاریخ تولید آنها گذاشته باشد استفاده نشود.
در مجموع تلقيح برنج در سه زمان امکان پذیر بوده که از کارایی متفاوتی برخوردار می باشند. این زمان ها شامل :
- زمان کاشت بذر در خزانه
- زمان نگهداری گیاه در خزانه
- زمان انتقال گیاه به مزرعه می باشد.
در صورتی که به لحاظ اقتصادی امکان تلقيح در هر سه مرحله باشد بهترین نتیجه حاصل خواهد شد. در غیر این صورت دو تلقیح تجمعی مرحله اول و سوم بیشترین تأثیر را خواهد داشت. پسی از آن تلقيح منفرد در مرحله اول و یا مرحله سوم از کارایی بیشتری برخوردار می باشند. روش تلقيح اضطرارى به صورت کود آبیاری در سطح بستر از کمترین تاثیر برخوردار خواهد بود .
3 – محلول پاشی:
نتایج آزمایشات سالهای اخیر نشان داده است کاربرد باکتریهای محرک رشد گیاه به صورت محلولپاشی دارای اثرات مثبتی در رشد و عملکرد گیاهان زراعی از جمله برنج است. برای این کار ابتدا با استفاده از یک سمپاشی مقدار آب مصرفی برای محلول پاشی مزرعه کالیبره می شود. محلول پاشى معمولاً در دو تا سه مرحله در دوره رشد سبزینه ای توصیه میشود. با توجه به سطح سبز مزرعه، مقدار کود زیستی مصرفی متفاوت خواهد بود. در روش محلول پاشی، به لحاظ اقتصادی می بایستی کود مورد نظر رقیق گردد. بر اساس جمعیت میکروارگانیسم مؤثر موجود در کود، رقیق سازی تا صد بار نیز مجاز میباشد. بهتر است از کودهای زیستی با جمعیت پایه ۱۰ به توان 7 و انواعی که بیش از دو ماه از تاریخ تولید آنها گذشته باشد استفاده نشود. محلول پاشی بهتر است در هنگام غروب آفتاب صورت گیرد تا ضمن جلوگیری از اثرات منفی امواج ماوراء بنفش نور خورشید، باکتریها از فرصت کافی برای نفود به فیلوسفر برخوردار باشند.
کودهای بیولوزیک محرک رشد گیاه با فرمولاسیون پودری
میزان مصرف کودهای زیستی پودری نیز بستگی به میزان و نوع بذر دارد. این کودها برای استقرار بهتر بر روی بذر نیازمند به استفاده از یک ماده چسباننده می باشند. بعضی از کمپانیهای معتبر در فرمولاسیون خود از مواد چسباننده استفاده کرده اند و در نتیجه در خصوص این کودها نیازی به ماده چسباننده وجود ندارد. ولی بیشتر تولید کننده ها یا در کنار کود خود این ماده چسباننده را قرار داده و یا مصرف کننده را به استفاده از ماده چسباننده راهنمایی می کنند. به منظور تلقیح بذر با کودهای پودری ابتدا بذر مورد نیاز به داخل ظرف مناسب تمیزی منتقل میشود. سپس متناسب با مقدار بذر درون ظرف، مقدار مشخصی از محلول ماده چسباننده به آن اضافه شده و به خوبی به هم زده می شود. پس از اطمینان کافی از چسبناک بودن کلیه بذور، کود زیستی اضافه شده و مجدداً به خوبی به هم زده می شود. در صورت امکان بهتر است قبل از کشت بذرها اندکی هوا خشک شده (در سایه و در سطح تمیز) و سپس کشت شوند. برای چسبناک کردن بذور از مواد متعددی استفاده می شود. محلول ۴۰ درصد صمغ عربی، ۲۰ درصد شکر، ۴ درصد متیل اتیل سلولز نمونه ای از این مواد می باشند. مقدار مواد چسباننده مصرفی بسیار مهم می باشد چرا که اگر ماده چسباننده بیش از نیاز اضافه گردد موجب چسبیدن بذرها به یکدیگر شده و در حالتی که کمتر از نیاز اضافه گردد مقدار کود اندکی را بر روی خود جای خواهد داد. در مورد برنج کاربرد ۵۰ میلی لیتر محلول چسباننده و حدود ۵۰ گرم مایه تلقیح پودری توصیه می گردد.
منابع
- بای بوردی، م؛ مج، ملکوتی، ه، امیرمکری و منفیسی، ۱۳۷۹، تولید و مصرف بهینه کود شیمیایی در راستای اهداف کشاورزی پایدار معاونت آموزش و تجهیز نیروی انسانی، سازمان تحقیقات، آموزش و ترویج کشاورزی، وزارت کشاورزی، کرج، ایران.
- ملکوتی، ۱۳۸۰. آزمون خاک: روش های تعیین حد بحرانی عناصر غذایی در خاک (قسمت دوم). نشریه فنی شماره ۲۳۳، شورای عالی توسعه کاربرد کودهای بیولوژیک و استفاده بهینه از کود و سم در کشاورزی، کرج، ایران.
- ملکوتی، ریاضی همدانی، ۱۳۷۰. کودها و حاصلخیزی خاک (ترجمه).
مرکز نشر دانشگاهی شماره ۵۹۸، تهران، ایران.
- Ali M. 1999. Evaluation of green manure technology in tropical lowland rice systems Field Crops Res 61.61–78.
- Armstrong W. 1967. The oxidizing activity of roots in waterlogged soils. Physiol Plant 20.920–926
- Balasubramanian V, Morales AC, Cruz RT, Abdulrachman S. 1999. Onfarm adaptation of knowledge-intensive nitrogen management technologies for rice systems Nutr Cycl Agroecosyst 53.59–69,
- Balasubramanian V, Morales AC, Cruz RT, Thiyagarajan TM, Nagarajan R, Babu M. Adulrachman S, Hai LH 2000. Adoption of the chlorophyll meter (SPAD) technology for real-time N management in rice a review. Int Rice Res. Notes 25 (1):4-8.
- Becker M, Ladha JK, Ali M. 1995. Green manure technology—potential, usage, and limitations—a case study for lowland rice. Plant Soil 174181–194
- Begg CBM, Kirk GID, Mackenzie AF, Neue HU 1994 Root-induced iron oxidation and pH changes in the rice rhizosphere. New Phytol 128469–477.
- Buresh RJ, De Datta SK 1990. Denitrification losses from puddled rice soils in the tropics Biol Fert soils 91—13.
- Buresh RJ, De Datta SK 1991. Nitrogen dynamics and management in rice-legume cropping systems. Adv. Agron 45:1-59
- Cassman KG, De Datta SK, Amarante ST, Liboon SP, Samson MI, Dizon MA 1996. Long-term comparison of agronomic efficiency and residual benefits of organic and inorganic nitrogen sources on irrigated lowland rice in the tropics Exp. Agric. 32.427–444,
- Crop and Resource Management Network (CREMNET). 2000. Farmer Participatory Approach to Nitrogen Management in Rice Production. Using the Leaf Color Chart (LCC). (CREMNET Technology Evaluation Protocol No. 1 (Revised Feb 2000). International Rice Research Institute (IRRI). Makati City 1271, Philippines.
- De Datta SK, Patrick WHJr. 1986. Nitrogen economy of flooded rice soils Developments in Plant and SoilSciences 26. The Hague. Martinus Nijhoff Publ.
- Fillery IRP, Vlek PLG 1986. Reappraisal of the significance of ammonia volatilization as an N loss mechanism in flooded rice fields Fert Res. 979–98
- Freney JR, Trevitt ACF, De Datta SK, Obcemea WN, Real JG 1990. The interdependence of ammonia volatilization and denitrification as nitrogen loss processes in flooded rice fields in the Philippines Biol Fert Soils 931–36
- George T, Buresh RJ, Ladha JK, Punzalan G. 1998. Recycling in situ of legume-fixed and soil nitrogen in tropical lowland rice. Agron J. 90.429–437.
18 George T, Ladha JK Gamity DP, Tomes RO 1995. Nitrogen dynamics of grain legume-weedy fallow-flooded rice sequences in the tropics. Agron J. 37:1–6
- Greenland DJ 1997. The sustainability of rice farming Oxon, Manila. CAB International and International Rice Research Institute
- Inoko A 1984. Compost as a source of plant nutrients. In Organic matter and rice. Manila (Philippines). International Rice Research Institute p 137–145
21, IRRI 1984. Organic matter and rice Manila (Philippines). International Rice Research Institute
22 Kirk GJD, Bajita JB. 1995. Root-induced iron oxidation, pH changes and zinc solubilization in the rhizosphere of lowland rice New Phytol 131:129– 137.
- Kirk GJD, Begg CBM, Solivas JL 1993. The chemistry of the lowland rice rhizosphere Plant Soil 155/156.83–86.
- Kirk GJD, Saleque MA 1995. Solubilization of phosphate by rice plants growing in reduced soil prediction of the amount solubilized and the resultant increase in uptake Eur J. SoilSci, 46.247-255.
- Kirk GJD, Solivas IL 1997. On the extent to which root properties and transport through the soil limit nitrogen uptake by lowland rice. Eur, J. Soil Sci. 48:613–621.
- Kumar A, Yadav DS. 1995. Use of organic manure and fertilizer in rice (Oryza sativa)—wheat (Triticum aestivum) cropping system for sustainability. Indian J. Agric Sci. 65.703–707 27. Ladha IK, Kundu DK, Coppenolle MGA, Peoples MB, Carangal VR, Dart PJ 1996. Legume productivity and soil nitrogen dynamics in lowland rice-based cropping systems SoilSci, Soc Am J 60.183–192
- Mikkelsen DS. 1987. Nitrogen budgets in flooded soils used for rice production Plant Soil 100.71–97
- Olk DC, Cassman KG, Mahieu N, RandallEW 1998. Conserved chemical properties of young soil humic acid fractions in tropical lowland soils under intensive irrigated rice cropping Eur, J. Soil Sci. 49:337-349
- Patnaik S, Panda D, Dash RN 1989. Long-term fertilizer experiments with vwetland rice Fert News 34(4):47—52.
- Patrick WH Jr. 1982 Nitrogen transformations in submerged soils. In Stevenson FJ, editor. Nitrogen in agricultural soils Agronomy 2. Madison, WI. American Society of Agronomy, SoilScience Society of America p 449–465
32. Patrick WH Jr., Delaune RD 1972 Characterization of the oxidized and reduced zones in flooded soils. Soil Sci. Soc. Am Proc. 36:573–576. - Peng S, Cassman KG, Kropff MJ 1995. Relationship between leaf photosynthesis and nitrogen content of field-grown rice in the tropics. CropSci 35:1627–1630.
- Peng S, Garcia FV, Laza MRC, Cassman KG 1993. Adjustment for specific leaf weight improves chlorophyll meter’s estimate of rice leaf nitrogen concentration Agron J 85987–990
35 Peng S, Garcia FV, Laza MRC, Sanico AL, Visperas RM, Cassman KG 1996 Increased N-use efficiency using a chlorophyll meter on high-yielding irrigated rice Field Crops Res 47.243–252 36. Peng S, Laza MRC, Garcia FV, Cassman KG 1995 Chlorophyll meter estimates leaf area-based nitrogen concentration of rice. Commun Soil Sci. Plant Anal. 26:927–935. 37. Ponnamperuma FN 1972. The chemistry of submerged soils. Adv. Agron 24:29–96.
- Ponnamperuma FN 1984. Straw as a source of nutrients for wetland rice In Organic matter and rice. Manila (Philippines). International Rice Research Institute. P 117–136.
- Qi-Xiao W. 1984. Utilization of organic materials in rice production in China. In Organic matter and rice. Manila (Philippines). International Rice Research Institute p 45–56
- Reddy KR, Patrick WH Jr. 1986 Fate of fertilizer nitrogen in the rice root zone. Soil Sci. Soc. Am J 50:649–651.
- Revsbech NP, Pedersen O, Reichardt W, Briones A. 1999. Microsensor analysis of oxygen and pH in the rice rhizosphere under field and laboratory conditions Biol. Fert Soils 29:379-385. 42 Roger PA 1996. Biology and management of the floodwater ecosystem in rice fields Manila (Philippines). International Rice Research Institutel ORSTOM
- Savant NK, De Datta SK 1982. Nitrogen transformations in wetland rice soils Adv. Agron 35:241-302
- Singh Y, Singh B, Maskina MS, Meelu OP. 1988. Effect of organic manures, crop residues, and green manure (Sesbania aculeata) on nitrogen and phosphorus transformations in a sandy loam soil at field capacity and under waterlogged conditions. Biol. Fertil Soils 6:1.83–187
- Tadano T, Yoshida S. 1978. Chemical changes in submerged soils and their effect on rice growth. In Soils and rice Los Ba (Philippines). International Rice Research Institute. p 399–420.
- Takai Y, Kamura T. 1966. The mechanisms of reduction in waterlogged paddy soil Folia Microbiol 11:304–313
- Takebe M. Yoneyama T 1989. Measurement of leaf color scores and its implication to nitrogen nutrition of rice plants. Jpn. Agric Res Q. 23.86–93.
48 Turner FT, Jund MF 1991. Chlorophyll meter to predict nitrogen topdress requirement for semidwarfrice Agron J 83.926–928.
- Turner FT, Jund MF 1994. Assessing the nitrogen requirements of rice crops with a chlorophyll meter Aust. J. Exp. Agr. 34.1001–1005.
50 Ventura WB, Ladha JK 1997. Sesbania phosphorus requirements when used as biofertilizer for long-term rice cultivation. Soil Sci Soc. Am J 61:1240–1244.
- Verma TS, Bhagat RM 1992 Impact of rice straw management practices on yield, nitrogen uptake, and soil properties in a wheat-rice rotation in northern India. Fert Res 33:97—106
- Vlek PLG, Byrnes BH 1986. The efficacy and loss of fertilizer N in lowland rice Fert Res 9:131—147
- Witt C, Cassman KG, Ottow JCG, Biker U. 1998. Soil microbial biomass and nitrogen supply in an irrigated lowland rice soil as affected by crop rotation and residue management Biol Fertil Soils 2871–80